검색결과
-
![[특집-기술위원회] TC 194 - 의료 장비의 생물학적 및 임상적 평가(Biological and clinical evaluation of medical devices)](http://www.stdnews.kr/data/file/news/thumb/thumb-3743812600_FrLCzJ0v_6a77c2077882a93f0804dbd4f16e6e8eefd439e0_200x180.jpg) [특집-기술위원회] TC 194 - 의료 장비의 생물학적 및 임상적 평가(Biological and clinical evaluation of medical devices)스위스 제네바에 본부를 두고 있는 국제표준화기구(ISO)에서 활동 중인 기술위원회(Technical Committeee, TC)는 TC 1~TC 323까지 구성돼 있다.기술위원회의 역할은 기술관리부가 승인한 작업범위 내 작업 프로그램 입안, 실행, 국제규격의 작성 등이다. 또한 산하 분과위원회(SC), 작업그룹(WG)을 통해 기타 ISO 기술위원회 또는 국제기관과 연계한다.ISO/IEC 기술작업 지침서 및 기술관리부 결정사항에 따른 ISO 국제규격안 작성·배포, 회원국의 의견 편집 등도 처리한다. 소속 분과위원회 및 작업그룹의 업무조정, 해당 기술위원회의 회의 준비도 담당한다.1947년 최초로 구성된 나사산에 대한 TC 1 기술위원회를 시작으로 순환경제를 표준화하기 위한 TC 323까지 각 TC 기술위원회의 의장, ISO 회원, 발행 표준 및 개발 표준 등에 대해 살펴볼 예정이다.이미 다룬 기술위원회와 구성 연도를 살펴 보면 △1947년 TC 1~TC 67 △1948년 TC 69 △1949년 TC 70~72 △1972년 TC 68 △1950년 TC 74 △1951년 TC 76 △1952년 TC 77 △1953년 TC 79, TC 81 △1955년 TC 82, TC 83 △1956년 TC 84, TC 85 △1957년 TC 86, TC 87, TC 89 △1958년 TC 91, TC 92 △1959년 TC 94 △1960년 TC 96, TC 98 △1961년 TC 101, TC 102, TC 104 등이다.또한 △1962년 TC 105~TC 107 △1963년 TC 108~TC 111 △1964년 TC 112~TC 115, TC 117 △1965년 TC 118 △1966년 TC 119~TC 122 △1967년 TC 123 △1968년 TC 126, TC 127 △1969년 TC 130~136 △1970년 TC 137, TC 138, TC 142, TC 145 △1971년 TC 146, TC 147, TC 148, TC 149, TC 150, TC 153 △1972년 TC 154 △1973년 TC 155 △1974년 TC 156~TC 161 △1975년 TC 162~TC 164 등도 포함된다.그리고 △1976년 TC 165, TC 166 △1977년 TC 167, TC 168, TC 170 △1978년 TC 171, TC 172, TC 173, TC 174 △1979년 TC 176, TC 178 △1980년 TC 180, TC 181 △1981년 TC 182 △1983년 TC 183~TC 186 △1984년 TC 188 △1985년 TC 189, TC 190, TC 191 등이 있다.ISO/TC 194 의료 장비의 생물학적 및 임상적 평가(Biological and clinical evaluation of medical devices)와 관련된 기술위원회는 TC 192, TC 193과 마찬가지로 1988년 결성됐다. 사무국은 독일 표준화기구(Deutsches Institut für Normung e.V., DIN)에서 맡고 있다.위원회는 수잔 민크위츠(Mrs Dr Susann Minkwitz)가 책임지고 있다. 현재 의장은 제레미 팅클러(Mr Jeremy Tinkler)이며 임기는 2026년 말까지다. ISO 기술 프로그램 관리자는 패트리샤 쿡(Mme Patricia Cook), ISO 편집 관리자는 산잘리 자인(Ms Sanjali Jain)등이다.범위는 해당 장치의 인간 임상 조사에 대한 우수 임상 실습 원칙 뿐 아니라 해당 재료 및 장치에 적용 가능한 생물학적 테스트 방법과 함께 의료 및 치과 재료 및 장치의 생물학적 및 임상 평가에 대한 접근 방식의 표준화다.현재 ISO/TC 194 사무국의 직접적인 책임 하에 발행된 표준은 37개 ISO/TC 194 사무국의 직접적인 책임 하에 개발 중인 표준은 16개다. 참여하고 있는 회원은 33개국, 참관 회원은 19개국이다.□ ISO/TC 194 사무국의 직접적인 책임 하에 발행된 표준 37개 중 15개 목록▷ISO 10993-1:2018 Biological evaluation of medical devices — Part 1: Evaluation and testing within a risk management process▷ISO 10993-2:2022 Biological evaluation of medical devices — Part 2: Animal welfare requirements▷ISO 10993-3:2014 Biological evaluation of medical devices — Part 3: Tests for genotoxicity, carcinogenicity and reproductive toxicity▷ISO 10993-4:2017 Biological evaluation of medical devices — Part 4: Selection of tests for interactions with blood▷ISO 10993-5:2009 Biological evaluation of medical devices — Part 5: Tests for in vitro cytotoxicity▷ISO 10993-6:2016 Biological evaluation of medical devices — Part 6: Tests for local effects after implantation▷ISO 10993-7:2008 Biological evaluation of medical devices — Part 7: Ethylene oxide sterilization residuals▷ISO 10993-7:2008/Amd 1:2019 Biological evaluation of medical devices — Part 7: Ethylene oxide sterilization residuals — Amendment 1: Applicability of allowable limits for neonates and infants▷ISO 10993-7:2008/Cor 1:2009 Biological evaluation of medical devices — Part 7: Ethylene oxide sterilization residuals — Technical Corrigendum 1▷ISO 10993-9:2019 Biological evaluation of medical devices — Part 9: Framework for identification and quantification of potential degradation products▷ISO 10993-10:2021 Biological evaluation of medical devices — Part 10: Tests for skin sensitization▷ISO 10993-11:2017 Biological evaluation of medical devices — Part 11: Tests for systemic toxicity▷ISO 10993-12:2021 Biological evaluation of medical devices — Part 12: Sample preparation and reference materials▷ISO 10993-13:2010 Biological evaluation of medical devices — Part 13: Identification and quantification of degradation products from polymeric medical devices▷ISO 10993-14:2001 Biological evaluation of medical devices — Part 14: Identification and quantification of degradation products from ceramics□ ISO/TC 194 사무국의 직접적인 책임 하에 개발 중인 표준 16개 목록▷ISO/CD 8250 Cleanliness of medical devices — Process design and test methods▷ISO/CD 10993-1.2 Biological evaluation of medical devices — Part 1: Requirements and general principles for the evaluation of biological safety within a risk management process▷ISO/AWI 10993-2 Biological evaluation of medical devices — Part 2: Animal welfare requirements▷ISO/AWI 10993-3 Biological evaluation of medical devices — Part 3: Tests for genotoxicity, carcinogenicity and reproductive toxicity▷ISO 10993-4:2017/DAmd 1 Biological evaluation of medical devices — Part 4: Selection of tests for interactions with blood — Amendment 1▷ISO/CD 10993-6 Biological evaluation of medical devices — Part 6: Tests for local effects after implantation▷ISO/CD 10993-7.2 Biological evaluation of medical devices — Part 7: Ethylene oxide sterilization residuals▷ISO/CD 10993-11 Biological evaluation of medical devices — Part 11: Tests for systemic toxicity▷ISO 10993-12:2021/AWI Amd 1 Biological evaluation of medical devices — Part 12: Sample preparation and reference materials — Amendment 1▷ISO/AWI 10993-16 Biological evaluation of medical devices — Part 16: Toxicokinetic study design for degradation products and leachables▷ISO 10993-17:2023/AWI Amd 1 Biological evaluation of medical devices — Part 17: Toxicological risk assessment of medical device constituents — Amendment 1▷ISO 10993-23:2021/AWI Amd 1 Biological evaluation of medical devices — Part 23: Tests for irritation — Amendment 1▷ISO/CD 14155 Clinical investigation of medical devices for human subjects — Good clinical practice▷ISO/AWI 18969 Clinical evaluation of medical devices▷ISO/AWI 21762 Medical devices utilizing human tissues and their derivatives — Application of risk management▷ISO/AWI TR 24850 Sources of hazard information for medical device constituents
[특집-기술위원회] TC 194 - 의료 장비의 생물학적 및 임상적 평가(Biological and clinical evaluation of medical devices)스위스 제네바에 본부를 두고 있는 국제표준화기구(ISO)에서 활동 중인 기술위원회(Technical Committeee, TC)는 TC 1~TC 323까지 구성돼 있다.기술위원회의 역할은 기술관리부가 승인한 작업범위 내 작업 프로그램 입안, 실행, 국제규격의 작성 등이다. 또한 산하 분과위원회(SC), 작업그룹(WG)을 통해 기타 ISO 기술위원회 또는 국제기관과 연계한다.ISO/IEC 기술작업 지침서 및 기술관리부 결정사항에 따른 ISO 국제규격안 작성·배포, 회원국의 의견 편집 등도 처리한다. 소속 분과위원회 및 작업그룹의 업무조정, 해당 기술위원회의 회의 준비도 담당한다.1947년 최초로 구성된 나사산에 대한 TC 1 기술위원회를 시작으로 순환경제를 표준화하기 위한 TC 323까지 각 TC 기술위원회의 의장, ISO 회원, 발행 표준 및 개발 표준 등에 대해 살펴볼 예정이다.이미 다룬 기술위원회와 구성 연도를 살펴 보면 △1947년 TC 1~TC 67 △1948년 TC 69 △1949년 TC 70~72 △1972년 TC 68 △1950년 TC 74 △1951년 TC 76 △1952년 TC 77 △1953년 TC 79, TC 81 △1955년 TC 82, TC 83 △1956년 TC 84, TC 85 △1957년 TC 86, TC 87, TC 89 △1958년 TC 91, TC 92 △1959년 TC 94 △1960년 TC 96, TC 98 △1961년 TC 101, TC 102, TC 104 등이다.또한 △1962년 TC 105~TC 107 △1963년 TC 108~TC 111 △1964년 TC 112~TC 115, TC 117 △1965년 TC 118 △1966년 TC 119~TC 122 △1967년 TC 123 △1968년 TC 126, TC 127 △1969년 TC 130~136 △1970년 TC 137, TC 138, TC 142, TC 145 △1971년 TC 146, TC 147, TC 148, TC 149, TC 150, TC 153 △1972년 TC 154 △1973년 TC 155 △1974년 TC 156~TC 161 △1975년 TC 162~TC 164 등도 포함된다.그리고 △1976년 TC 165, TC 166 △1977년 TC 167, TC 168, TC 170 △1978년 TC 171, TC 172, TC 173, TC 174 △1979년 TC 176, TC 178 △1980년 TC 180, TC 181 △1981년 TC 182 △1983년 TC 183~TC 186 △1984년 TC 188 △1985년 TC 189, TC 190, TC 191 등이 있다.ISO/TC 194 의료 장비의 생물학적 및 임상적 평가(Biological and clinical evaluation of medical devices)와 관련된 기술위원회는 TC 192, TC 193과 마찬가지로 1988년 결성됐다. 사무국은 독일 표준화기구(Deutsches Institut für Normung e.V., DIN)에서 맡고 있다.위원회는 수잔 민크위츠(Mrs Dr Susann Minkwitz)가 책임지고 있다. 현재 의장은 제레미 팅클러(Mr Jeremy Tinkler)이며 임기는 2026년 말까지다. ISO 기술 프로그램 관리자는 패트리샤 쿡(Mme Patricia Cook), ISO 편집 관리자는 산잘리 자인(Ms Sanjali Jain)등이다.범위는 해당 장치의 인간 임상 조사에 대한 우수 임상 실습 원칙 뿐 아니라 해당 재료 및 장치에 적용 가능한 생물학적 테스트 방법과 함께 의료 및 치과 재료 및 장치의 생물학적 및 임상 평가에 대한 접근 방식의 표준화다.현재 ISO/TC 194 사무국의 직접적인 책임 하에 발행된 표준은 37개 ISO/TC 194 사무국의 직접적인 책임 하에 개발 중인 표준은 16개다. 참여하고 있는 회원은 33개국, 참관 회원은 19개국이다.□ ISO/TC 194 사무국의 직접적인 책임 하에 발행된 표준 37개 중 15개 목록▷ISO 10993-1:2018 Biological evaluation of medical devices — Part 1: Evaluation and testing within a risk management process▷ISO 10993-2:2022 Biological evaluation of medical devices — Part 2: Animal welfare requirements▷ISO 10993-3:2014 Biological evaluation of medical devices — Part 3: Tests for genotoxicity, carcinogenicity and reproductive toxicity▷ISO 10993-4:2017 Biological evaluation of medical devices — Part 4: Selection of tests for interactions with blood▷ISO 10993-5:2009 Biological evaluation of medical devices — Part 5: Tests for in vitro cytotoxicity▷ISO 10993-6:2016 Biological evaluation of medical devices — Part 6: Tests for local effects after implantation▷ISO 10993-7:2008 Biological evaluation of medical devices — Part 7: Ethylene oxide sterilization residuals▷ISO 10993-7:2008/Amd 1:2019 Biological evaluation of medical devices — Part 7: Ethylene oxide sterilization residuals — Amendment 1: Applicability of allowable limits for neonates and infants▷ISO 10993-7:2008/Cor 1:2009 Biological evaluation of medical devices — Part 7: Ethylene oxide sterilization residuals — Technical Corrigendum 1▷ISO 10993-9:2019 Biological evaluation of medical devices — Part 9: Framework for identification and quantification of potential degradation products▷ISO 10993-10:2021 Biological evaluation of medical devices — Part 10: Tests for skin sensitization▷ISO 10993-11:2017 Biological evaluation of medical devices — Part 11: Tests for systemic toxicity▷ISO 10993-12:2021 Biological evaluation of medical devices — Part 12: Sample preparation and reference materials▷ISO 10993-13:2010 Biological evaluation of medical devices — Part 13: Identification and quantification of degradation products from polymeric medical devices▷ISO 10993-14:2001 Biological evaluation of medical devices — Part 14: Identification and quantification of degradation products from ceramics□ ISO/TC 194 사무국의 직접적인 책임 하에 개발 중인 표준 16개 목록▷ISO/CD 8250 Cleanliness of medical devices — Process design and test methods▷ISO/CD 10993-1.2 Biological evaluation of medical devices — Part 1: Requirements and general principles for the evaluation of biological safety within a risk management process▷ISO/AWI 10993-2 Biological evaluation of medical devices — Part 2: Animal welfare requirements▷ISO/AWI 10993-3 Biological evaluation of medical devices — Part 3: Tests for genotoxicity, carcinogenicity and reproductive toxicity▷ISO 10993-4:2017/DAmd 1 Biological evaluation of medical devices — Part 4: Selection of tests for interactions with blood — Amendment 1▷ISO/CD 10993-6 Biological evaluation of medical devices — Part 6: Tests for local effects after implantation▷ISO/CD 10993-7.2 Biological evaluation of medical devices — Part 7: Ethylene oxide sterilization residuals▷ISO/CD 10993-11 Biological evaluation of medical devices — Part 11: Tests for systemic toxicity▷ISO 10993-12:2021/AWI Amd 1 Biological evaluation of medical devices — Part 12: Sample preparation and reference materials — Amendment 1▷ISO/AWI 10993-16 Biological evaluation of medical devices — Part 16: Toxicokinetic study design for degradation products and leachables▷ISO 10993-17:2023/AWI Amd 1 Biological evaluation of medical devices — Part 17: Toxicological risk assessment of medical device constituents — Amendment 1▷ISO 10993-23:2021/AWI Amd 1 Biological evaluation of medical devices — Part 23: Tests for irritation — Amendment 1▷ISO/CD 14155 Clinical investigation of medical devices for human subjects — Good clinical practice▷ISO/AWI 18969 Clinical evaluation of medical devices▷ISO/AWI 21762 Medical devices utilizing human tissues and their derivatives — Application of risk management▷ISO/AWI TR 24850 Sources of hazard information for medical device constituents -
 식약처, 생물학적 제제 등 보관 및 수송 관리 가이드라인 개정식품의약품안전처는 생물학적 제제 등의 보관·수송 관리 합리화에 따른 운영방안 등을 상세하게 안내하기 위해 ‘생물학적 제제 등 보관 및 수송 관리 가이드라인’을 12월 28일 개정했다고 밝혔다. 생물학적 제제 등은 생물학적 제제(백신, 혈장분획제제 및 항독소), 유전자재조합의약품, 세포배양의약품, 세포치료제, 유전자 치료제 및 이와 유사한 제제를 말한다. 이번 개정 가이드라인으로 올바른 바이오의약품 수송과 보관 관리에 도움이 될 것으로 기대된다. 주요 개정 내용은 ▲보관온도에 따른 제품군별 수송 관리 방법 안내 ▲일시적 온도 일탈 시 과학적 입증 방법 안내 ▲제품 수송 시 온도관리 등에 관한 질의응답 사항 등이다. 식약처 관계자는 “이번 개정 가이드라인에서는 생물학적 제제 등을 취급하는 제조·수입 업체와 도매상이 개정된 법령에 따라 준수해야 하는 사항을 실무 운영 측면에서 어떻게 적용해야 하는지 자세하게 설명했다”며 “바이오의약품의 유통체계를 고려한 온도관리 방법 등도 상세하게 안내했다”고 설명했다. 식약처는 이번 개정 가이드라인이 올바른 바이오의약품 수송과 보관 관리에 도움을 줄 것으로 기대하며, 앞으로도 안전한 바이오의약품을 공급하기 위해 최선을 다하겠다고 밝혔다. 자세한 내용은 식약처 누리집(mfds.go.kr) > 법령/자료 > 법령정보 > 공무원지침서/민원인안내서에서 확인할 수 있다.
식약처, 생물학적 제제 등 보관 및 수송 관리 가이드라인 개정식품의약품안전처는 생물학적 제제 등의 보관·수송 관리 합리화에 따른 운영방안 등을 상세하게 안내하기 위해 ‘생물학적 제제 등 보관 및 수송 관리 가이드라인’을 12월 28일 개정했다고 밝혔다. 생물학적 제제 등은 생물학적 제제(백신, 혈장분획제제 및 항독소), 유전자재조합의약품, 세포배양의약품, 세포치료제, 유전자 치료제 및 이와 유사한 제제를 말한다. 이번 개정 가이드라인으로 올바른 바이오의약품 수송과 보관 관리에 도움이 될 것으로 기대된다. 주요 개정 내용은 ▲보관온도에 따른 제품군별 수송 관리 방법 안내 ▲일시적 온도 일탈 시 과학적 입증 방법 안내 ▲제품 수송 시 온도관리 등에 관한 질의응답 사항 등이다. 식약처 관계자는 “이번 개정 가이드라인에서는 생물학적 제제 등을 취급하는 제조·수입 업체와 도매상이 개정된 법령에 따라 준수해야 하는 사항을 실무 운영 측면에서 어떻게 적용해야 하는지 자세하게 설명했다”며 “바이오의약품의 유통체계를 고려한 온도관리 방법 등도 상세하게 안내했다”고 설명했다. 식약처는 이번 개정 가이드라인이 올바른 바이오의약품 수송과 보관 관리에 도움을 줄 것으로 기대하며, 앞으로도 안전한 바이오의약품을 공급하기 위해 최선을 다하겠다고 밝혔다. 자세한 내용은 식약처 누리집(mfds.go.kr) > 법령/자료 > 법령정보 > 공무원지침서/민원인안내서에서 확인할 수 있다. -
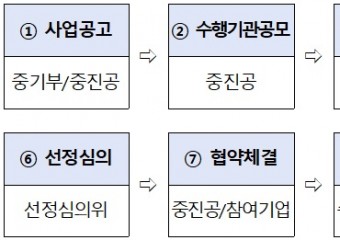
 12개의 국가전략기술 선정, 기술패권 경쟁에서 우위 노린다정부는 12월 20일 「국가전략기술 선정(안)」을 심의·의결하고, 우리나라의 기술패권 경쟁에서 선도적인 역할을 수행할 '12대 국가전략기술'을 확정했다. 이는 '제1차 국가과학기술자문회의 전원회의'를 통해 공급망·신산업·외교안보 관점에서 전략적 가치가 높다고 판단된 분야들이다. 정부는 이를 중점으로 예산 투자와 함께 '임무중심 전략로드맵' 수립하고 '국가전략기술 프로젝트'를 추진할 계획이다. 이에 따라 선정된 12대 국가전략기술은 반도체·디스플레이, 이차전지, 첨단 모빌리티, 차세대 원자력, 첨단 바이오, 우주항공·해양, 수소, 사이버보안, 인공지능, 차세대 통신, 첨단로봇·제조, 양자 등이다. 이로써 초격차 기술을 확보하기 위한 정부의 의지와 투자가 명확한 방향으로 나아가고 있다. 뿐만 아니라 「국가전략기술 육성에 관한 특별법」의 제정과 시행으로 범부처 차원에서의 법적 근거가 마련되었다. 정부는 12대 분야를 국가전략기술로 공식 지정하고, 이에 추가로 AI반도체, 합성생물학 등 50개의 중점기술을 선정하고 그 세부 정의를 구체화했다. 선정된 국가전략기술은 과기정통부 장관 고시로 최종 확정될 예정이며, 특별법에 따른 다양한 정책적 지원수단과 혁신적인 연구개발을 통해 초격차 기술을 확보할 계획이다. 주영창 과학기술혁신본부장은 "초격차 전략기술 확보는 국가생존의 핵심"이라며 "세계 최고에 도전하는 혁신·도전적 연구개발을 통해 국가를 주도하는 역할을 수행할 것"이라고 밝혔다.
12개의 국가전략기술 선정, 기술패권 경쟁에서 우위 노린다정부는 12월 20일 「국가전략기술 선정(안)」을 심의·의결하고, 우리나라의 기술패권 경쟁에서 선도적인 역할을 수행할 '12대 국가전략기술'을 확정했다. 이는 '제1차 국가과학기술자문회의 전원회의'를 통해 공급망·신산업·외교안보 관점에서 전략적 가치가 높다고 판단된 분야들이다. 정부는 이를 중점으로 예산 투자와 함께 '임무중심 전략로드맵' 수립하고 '국가전략기술 프로젝트'를 추진할 계획이다. 이에 따라 선정된 12대 국가전략기술은 반도체·디스플레이, 이차전지, 첨단 모빌리티, 차세대 원자력, 첨단 바이오, 우주항공·해양, 수소, 사이버보안, 인공지능, 차세대 통신, 첨단로봇·제조, 양자 등이다. 이로써 초격차 기술을 확보하기 위한 정부의 의지와 투자가 명확한 방향으로 나아가고 있다. 뿐만 아니라 「국가전략기술 육성에 관한 특별법」의 제정과 시행으로 범부처 차원에서의 법적 근거가 마련되었다. 정부는 12대 분야를 국가전략기술로 공식 지정하고, 이에 추가로 AI반도체, 합성생물학 등 50개의 중점기술을 선정하고 그 세부 정의를 구체화했다. 선정된 국가전략기술은 과기정통부 장관 고시로 최종 확정될 예정이며, 특별법에 따른 다양한 정책적 지원수단과 혁신적인 연구개발을 통해 초격차 기술을 확보할 계획이다. 주영창 과학기술혁신본부장은 "초격차 전략기술 확보는 국가생존의 핵심"이라며 "세계 최고에 도전하는 혁신·도전적 연구개발을 통해 국가를 주도하는 역할을 수행할 것"이라고 밝혔다. -
 FITI시험연구원, ‘2023 FITI 안전의 날’ 행사 개최FITI시험연구원은 21일 서울 본원에서 ‘2023 FITI 안전의 날’ 행사를 개최했다고 밝혔다. ‘FITI 안전의 날’ 행사는 안전에 대한 직원들의 관심을 유도해 안전 문화를 확산하고 연구실 안전 인식을 제고하기 위한 자리로 올해 처음 마련됐다. 지난해 안전보건 경영방침을 선포한 후 FITI시험연구원의 안전보건 목표인 ‘365일, 24시간 사고 ZERO FITI’를 달성하기 위해 전 직원이 안전 확보를 실천하고 있다. 이번 행사는 김화영 FITI시험연구원장, 김홍관 FITI시험연구원 부원장 등이 참석한 가운데, 안전관리 시상식, 특별강연, 간담회 등으로 진행됐다. 먼저 연구원 안전 확보에 기여한 부서 및 개인의 시상이 열려 역학성능평가팀, 대구시험인증센터 등 6개 안전관리 우수부서와 연구실안전관리사 자격 취득자 포상이 이뤄졌다. 또한 안전 콘텐츠 공모전을 통해 포스터, 마스코트, 캐치프레이즈, UCC 부문에서 접수된 61개 작품 중 당선작 19개에 대한 시상식도 가졌다. 이날 ‘연구실 안전관리 및 설치운영 가이드’를 주제로 대전과학기술대학교 소방·산업안전관리학과 송영호 교수의 특별강연과 연구실 안전관리담당자 간담회가 진행돼 연구실 안전보건 관리 전반에 대해 심도 있게 논의했다. 김화영 FITI시험연구원장은 “FITI 안전의 날을 맞아 진행된 다양한 프로그램을 통해 안전에 대한 중요성을 다시금 되새기는 시간이 됐다”며 “2024년에도 철저한 안전보건계획을 수립해 더욱 안전한 FITI시험연구원이 될 것을 약속드린다”고 전했다. 한편 FITI시험연구원은 정부로부터 4년 연속 연구실 안전관리 우수성을 인정받아 안전관리 우수연구실 6곳을 보유하고 있다. 그중 보호구 생물학적 안전성 평가 시험실은 안전관리 최우수 연구실로 선정돼 우수한 안전관리 시스템과 높은 안전의식 수준을 자랑했다.
FITI시험연구원, ‘2023 FITI 안전의 날’ 행사 개최FITI시험연구원은 21일 서울 본원에서 ‘2023 FITI 안전의 날’ 행사를 개최했다고 밝혔다. ‘FITI 안전의 날’ 행사는 안전에 대한 직원들의 관심을 유도해 안전 문화를 확산하고 연구실 안전 인식을 제고하기 위한 자리로 올해 처음 마련됐다. 지난해 안전보건 경영방침을 선포한 후 FITI시험연구원의 안전보건 목표인 ‘365일, 24시간 사고 ZERO FITI’를 달성하기 위해 전 직원이 안전 확보를 실천하고 있다. 이번 행사는 김화영 FITI시험연구원장, 김홍관 FITI시험연구원 부원장 등이 참석한 가운데, 안전관리 시상식, 특별강연, 간담회 등으로 진행됐다. 먼저 연구원 안전 확보에 기여한 부서 및 개인의 시상이 열려 역학성능평가팀, 대구시험인증센터 등 6개 안전관리 우수부서와 연구실안전관리사 자격 취득자 포상이 이뤄졌다. 또한 안전 콘텐츠 공모전을 통해 포스터, 마스코트, 캐치프레이즈, UCC 부문에서 접수된 61개 작품 중 당선작 19개에 대한 시상식도 가졌다. 이날 ‘연구실 안전관리 및 설치운영 가이드’를 주제로 대전과학기술대학교 소방·산업안전관리학과 송영호 교수의 특별강연과 연구실 안전관리담당자 간담회가 진행돼 연구실 안전보건 관리 전반에 대해 심도 있게 논의했다. 김화영 FITI시험연구원장은 “FITI 안전의 날을 맞아 진행된 다양한 프로그램을 통해 안전에 대한 중요성을 다시금 되새기는 시간이 됐다”며 “2024년에도 철저한 안전보건계획을 수립해 더욱 안전한 FITI시험연구원이 될 것을 약속드린다”고 전했다. 한편 FITI시험연구원은 정부로부터 4년 연속 연구실 안전관리 우수성을 인정받아 안전관리 우수연구실 6곳을 보유하고 있다. 그중 보호구 생물학적 안전성 평가 시험실은 안전관리 최우수 연구실로 선정돼 우수한 안전관리 시스템과 높은 안전의식 수준을 자랑했다. -
 FITI시험연구원, ‘2023년 안전관리 최우수 연구실’ 선정FITI시험연구원은 보호구 생물학적 안전성 평가 시험실이 과학기술정보통신부 주관 ‘2023년 안전관리 우수연구실 인증제’에서 ‘안전관리 최우수 연구실’로 선정됐다고 6일 밝혔다. 안전관리 우수연구실 인증제는 과학기술 분야 연구실의 안전관리 수준과 활동 등이 우수한 곳을 대상으로 전문가 심사를 통해 정부가 인증을 부여하는 제도다. 인증을 받기 위해서는 최근 2년 이내 사고가 없어야 하며 ▲안전환경 시스템 ▲안전환경 활동수준 ▲안전관리 관계자 안전의식 등 3가지 분야에서 80점 이상의 점수를 획득해야 한다. 이 가운데 가장 모범적이고 안전문화 확산에 이바지한 연구실은 최우수 연구실로 선정된다. 이번 심사에서 FITI시험연구원은 보호구 생물학적 안전성 평가 시험실, 드라이클리닝 시험실 등 2곳에 대한 신규 인증을 획득했다. 그중 보호구 생물학적 안전성 평가 시험실은 FITI시험연구원 첫 안전관리 최우수 연구실로 선정됐다. 보호구 생물학적 안전성 평가 시험실은 감염 보호복의 차단 성능을 시험하는 공간으로 인공혈액, 박테리오파지, 건식·습식 미생물 등의 침투 저항성을 평가해 안전관리에 각별한 주의가 필요하다. 이에 생물안전관리지침을 제정하고 생물안전작업대(BSC) 등 안전장비를 구축해 생물안전 2등급(BSL-2)에 준하는 시설로 관리, 시험연구시설의 안전성 확보에 노력을 기울이고 있다. FITI시험연구원은 지난 2020년 무기분석실, 2021년 유기전처리실, GC실, 2022년 습식분석실에 이어 4년 연속 연구실 안전관리 우수성을 입증해 안전관리 우수연구실 총 6곳을 보유하게 됐다. 김화영 FITI시험연구원장은 “이번 인증을 통해 그동안 FITI시험연구원 연구원들이 구축해 온 우수한 안전관리 시스템과 높은 안전의식 수준을 대외적으로 인정받았다”며 “앞으로도 원내 안전관리 체계를 고도화하고 자율적인 안전문화를 정착시켜 더 안전한 환경을 조성하겠다”고 전했다.
FITI시험연구원, ‘2023년 안전관리 최우수 연구실’ 선정FITI시험연구원은 보호구 생물학적 안전성 평가 시험실이 과학기술정보통신부 주관 ‘2023년 안전관리 우수연구실 인증제’에서 ‘안전관리 최우수 연구실’로 선정됐다고 6일 밝혔다. 안전관리 우수연구실 인증제는 과학기술 분야 연구실의 안전관리 수준과 활동 등이 우수한 곳을 대상으로 전문가 심사를 통해 정부가 인증을 부여하는 제도다. 인증을 받기 위해서는 최근 2년 이내 사고가 없어야 하며 ▲안전환경 시스템 ▲안전환경 활동수준 ▲안전관리 관계자 안전의식 등 3가지 분야에서 80점 이상의 점수를 획득해야 한다. 이 가운데 가장 모범적이고 안전문화 확산에 이바지한 연구실은 최우수 연구실로 선정된다. 이번 심사에서 FITI시험연구원은 보호구 생물학적 안전성 평가 시험실, 드라이클리닝 시험실 등 2곳에 대한 신규 인증을 획득했다. 그중 보호구 생물학적 안전성 평가 시험실은 FITI시험연구원 첫 안전관리 최우수 연구실로 선정됐다. 보호구 생물학적 안전성 평가 시험실은 감염 보호복의 차단 성능을 시험하는 공간으로 인공혈액, 박테리오파지, 건식·습식 미생물 등의 침투 저항성을 평가해 안전관리에 각별한 주의가 필요하다. 이에 생물안전관리지침을 제정하고 생물안전작업대(BSC) 등 안전장비를 구축해 생물안전 2등급(BSL-2)에 준하는 시설로 관리, 시험연구시설의 안전성 확보에 노력을 기울이고 있다. FITI시험연구원은 지난 2020년 무기분석실, 2021년 유기전처리실, GC실, 2022년 습식분석실에 이어 4년 연속 연구실 안전관리 우수성을 입증해 안전관리 우수연구실 총 6곳을 보유하게 됐다. 김화영 FITI시험연구원장은 “이번 인증을 통해 그동안 FITI시험연구원 연구원들이 구축해 온 우수한 안전관리 시스템과 높은 안전의식 수준을 대외적으로 인정받았다”며 “앞으로도 원내 안전관리 체계를 고도화하고 자율적인 안전문화를 정착시켜 더 안전한 환경을 조성하겠다”고 전했다. -
 식약처, ‘생물학적제제 품질관리실험실 네트워크(Lab-Net) 워크숍’ 개최식품의약품안전처는 백신·혈장분획제제 품질관리에 대한 최신 기술정보를 공유하는 ‘2023년 생물학적제제 품질관리실험실 네트워크(Lab-Net) 워크숍’을 23일 오송 C&V센터에서 개최한다고 밝혔다. 이번 워크숍으로 백신·혈장분획제제 업계의 품질관리 역량을 강화하는 데 도움이 될 것으로 기대된다. ‘생물학적제제 품질관리실험실 네트워크(Lab-Net)’는 식약처와 백신·혈장분획제제 제조·수입업체, 품질 검사기관 등이 참여하는 민·관 협의체로 2011년에 출범한 이후 품질관리 분야에서 활발하게 교류하며 국내 백신, 혈장분획제제 품질을 높이는 데 기여해 왔다. 이번 워크숍은 전문가 강연과 2023년 Lab-Net 운영 현황 및 내년도 계획 등에 대한 발표로 구성돼 있다. 전문가 초청 강연에서는 ▲시험방법 밸리데이션을 위한 통계 방법 ▲미국약전 생물학적 정량법 밸리데이션 ▲데이터 완전성과 컴퓨터 시스템 밸리데이션 ▲오염 관리 전략 수립 접근방법 등을 소개한다. 아울러 ▲백신 역가 시험법 개선 ▲항트롬빈III제제국가표준품 확립공동연구 ▲혈장분획제제 동물대체시험법 추진 등 Lab-Net 운영 성과와 내년도 계획에 대해서도 안내한다. 식약처 관계자는 “이번 워크숍이 백신·혈장분획제제 업계의 품질관리 역량을 강화하는 데 도움을 줄 것으로 기대한다”며 “앞으로도 전문성과 규제과학에 기반한 철저한 품질관리를 수행하여 안전한 제품이 국민께 공급될 수 있도록 최선을 다해 노력할 계획”이라고 밝혔다.
식약처, ‘생물학적제제 품질관리실험실 네트워크(Lab-Net) 워크숍’ 개최식품의약품안전처는 백신·혈장분획제제 품질관리에 대한 최신 기술정보를 공유하는 ‘2023년 생물학적제제 품질관리실험실 네트워크(Lab-Net) 워크숍’을 23일 오송 C&V센터에서 개최한다고 밝혔다. 이번 워크숍으로 백신·혈장분획제제 업계의 품질관리 역량을 강화하는 데 도움이 될 것으로 기대된다. ‘생물학적제제 품질관리실험실 네트워크(Lab-Net)’는 식약처와 백신·혈장분획제제 제조·수입업체, 품질 검사기관 등이 참여하는 민·관 협의체로 2011년에 출범한 이후 품질관리 분야에서 활발하게 교류하며 국내 백신, 혈장분획제제 품질을 높이는 데 기여해 왔다. 이번 워크숍은 전문가 강연과 2023년 Lab-Net 운영 현황 및 내년도 계획 등에 대한 발표로 구성돼 있다. 전문가 초청 강연에서는 ▲시험방법 밸리데이션을 위한 통계 방법 ▲미국약전 생물학적 정량법 밸리데이션 ▲데이터 완전성과 컴퓨터 시스템 밸리데이션 ▲오염 관리 전략 수립 접근방법 등을 소개한다. 아울러 ▲백신 역가 시험법 개선 ▲항트롬빈III제제국가표준품 확립공동연구 ▲혈장분획제제 동물대체시험법 추진 등 Lab-Net 운영 성과와 내년도 계획에 대해서도 안내한다. 식약처 관계자는 “이번 워크숍이 백신·혈장분획제제 업계의 품질관리 역량을 강화하는 데 도움을 줄 것으로 기대한다”며 “앞으로도 전문성과 규제과학에 기반한 철저한 품질관리를 수행하여 안전한 제품이 국민께 공급될 수 있도록 최선을 다해 노력할 계획”이라고 밝혔다. -
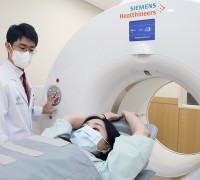 서울아산병원 유방암 영상진단법, 세계 표준검사로국내 의료진이 연구한 유방암 환자의 여성호르몬 수용체 영상진단법이 전 세계의 표준검사가 됐다. 조직검사가 어려웠던 환자들도 15분 내외의 영상검사만으로 진단이 가능해져 보다 편하고 안전하게 여성호르몬 수용체 진단을 받을 수 있게 됐다. ᅠ 서울아산병원은 유방암센터가 안전성과 유효성을 처음 입증한 ‘18F-FES 양전자방출단층촬영(PET)’ 검사가 세계적 암 치료 기준을 선도하는 미국종합암네트워크의 가이드라인으로 최근 발표됐다고 14일 밝혔다. ᅠ 유방암은 여성호르몬 수용체 여부에 따라 치료법이 달라지기 때문에 정확하게 진단하는 것이 중요하다. 재발이나 전이된 유방암 환자의 여성호르몬 수용체 여부를 진단할 때 18F-FES PET 검사를 시행하도록 권고하는 가이드라인이 발표된 것이다. ᅠ F-FES PET 검사는 여성호르몬인 에스트로겐 수용체의 생물학적 활성을 측정할 수 있는 18F-FES 약물을 주입한 뒤 PET 검사를 통해 유방암 여성호르몬 수용체를 진단하는 검사다. 조직검사가 어렵거나 불가능한 경우 영상촬영만으로 통증 없이 정확하고 안전하게 진단이 가능하다. ᅠ 유방암은 여성호르몬 수용체 여부에 따라 치료법이 달라진다. 우리나라 유방암 환자 70%에 해당하는 여성호르몬 수용체 양성 유방암은 호르몬에 의해 암세포가 성장하기 때문에 항호르몬 치료가 필요하다. ᅠ 유방암이 재발하거나 전이된 경우에도, 여성호르몬 수용체 진단 결과에 따라 치료방법이 결정되기 때문에 추가적인 조직검사가 필요하다. 이때 재발한 부위가 여러 군데이거나 전이된 위치에 따라 조직검사가 어렵거나 불가능할 수 있는데, 이러한 경우 18F-FES PET 검사가 표준 진단검사의 하나로 사용되도록 권고된 것이다. ᅠ F-FES PET 검사는 간단한 영상촬영만으로 몸 전체에 전이된 병변을 한 번에 검사할 수 있으며, 소요시간은 15분 내외로 아주 짧다. 통증도 없어 환자들이 조직검사에 대한 부담을 덜 수 있게 됐다. ᅠ 서울아산병원 유방암센터는 18F-FES PET 검사의 개발 및 임상을 주도적으로 진행했으며, 이러한 연구 결과는 미국핵의학회 및 대한핵의학회가 18F-FES PET 검사의 적정이용기준을 발표할 때 주요 근거로 채택되기도 했다. ᅠ 김성배 서울아산병원 유방암센터소장은 “18F-FES PET 등과 같은 유방암 진단 기술 발전에 더불어 항암제, 항호르몬, 방사선 등 치료법도 점차 발전하면서 유방암 5년 생존율 95%를 바라보고 있다”고 설명했다. 이어 “특히 여성호르몬 수용체 양성 유방암은 유방암 중에서도 늦은 재발 위험이 상대적으로 높고 수용체가 변하기도 하지만, 환자분들이 희망을 놓지 않고 적극적으로 치료에 임하면 좋은 결과를 얻을 수 있을 것”이라고 언급했다. 문대혁 서울아산병원 핵의학과 교수는 “우리나라에서 연구를 진행해 안전성과 유효성이 입증된 18F-FES PET 검사가 미국종합암네트워크 가이드라인으로 권고되어 매우 기쁘게 생각한다”며 “조직검사가 어렵거나 불가능했던 재발 혹은 전이된 전 세계의 유방암 환자들이 더욱 안전하고 정확하게 여성호르몬 수용체 여부를 진단받고 가장 적절한 치료를 받을 수 있을 것으로 기대된다”고 말했다. 이어 “앞으로도 암환자들의 생존율을 높이고 맞춤 치료를 제공하기 위한 글로벌 연구를 주도해 나가겠다”고 덧붙였다.
서울아산병원 유방암 영상진단법, 세계 표준검사로국내 의료진이 연구한 유방암 환자의 여성호르몬 수용체 영상진단법이 전 세계의 표준검사가 됐다. 조직검사가 어려웠던 환자들도 15분 내외의 영상검사만으로 진단이 가능해져 보다 편하고 안전하게 여성호르몬 수용체 진단을 받을 수 있게 됐다. ᅠ 서울아산병원은 유방암센터가 안전성과 유효성을 처음 입증한 ‘18F-FES 양전자방출단층촬영(PET)’ 검사가 세계적 암 치료 기준을 선도하는 미국종합암네트워크의 가이드라인으로 최근 발표됐다고 14일 밝혔다. ᅠ 유방암은 여성호르몬 수용체 여부에 따라 치료법이 달라지기 때문에 정확하게 진단하는 것이 중요하다. 재발이나 전이된 유방암 환자의 여성호르몬 수용체 여부를 진단할 때 18F-FES PET 검사를 시행하도록 권고하는 가이드라인이 발표된 것이다. ᅠ F-FES PET 검사는 여성호르몬인 에스트로겐 수용체의 생물학적 활성을 측정할 수 있는 18F-FES 약물을 주입한 뒤 PET 검사를 통해 유방암 여성호르몬 수용체를 진단하는 검사다. 조직검사가 어렵거나 불가능한 경우 영상촬영만으로 통증 없이 정확하고 안전하게 진단이 가능하다. ᅠ 유방암은 여성호르몬 수용체 여부에 따라 치료법이 달라진다. 우리나라 유방암 환자 70%에 해당하는 여성호르몬 수용체 양성 유방암은 호르몬에 의해 암세포가 성장하기 때문에 항호르몬 치료가 필요하다. ᅠ 유방암이 재발하거나 전이된 경우에도, 여성호르몬 수용체 진단 결과에 따라 치료방법이 결정되기 때문에 추가적인 조직검사가 필요하다. 이때 재발한 부위가 여러 군데이거나 전이된 위치에 따라 조직검사가 어렵거나 불가능할 수 있는데, 이러한 경우 18F-FES PET 검사가 표준 진단검사의 하나로 사용되도록 권고된 것이다. ᅠ F-FES PET 검사는 간단한 영상촬영만으로 몸 전체에 전이된 병변을 한 번에 검사할 수 있으며, 소요시간은 15분 내외로 아주 짧다. 통증도 없어 환자들이 조직검사에 대한 부담을 덜 수 있게 됐다. ᅠ 서울아산병원 유방암센터는 18F-FES PET 검사의 개발 및 임상을 주도적으로 진행했으며, 이러한 연구 결과는 미국핵의학회 및 대한핵의학회가 18F-FES PET 검사의 적정이용기준을 발표할 때 주요 근거로 채택되기도 했다. ᅠ 김성배 서울아산병원 유방암센터소장은 “18F-FES PET 등과 같은 유방암 진단 기술 발전에 더불어 항암제, 항호르몬, 방사선 등 치료법도 점차 발전하면서 유방암 5년 생존율 95%를 바라보고 있다”고 설명했다. 이어 “특히 여성호르몬 수용체 양성 유방암은 유방암 중에서도 늦은 재발 위험이 상대적으로 높고 수용체가 변하기도 하지만, 환자분들이 희망을 놓지 않고 적극적으로 치료에 임하면 좋은 결과를 얻을 수 있을 것”이라고 언급했다. 문대혁 서울아산병원 핵의학과 교수는 “우리나라에서 연구를 진행해 안전성과 유효성이 입증된 18F-FES PET 검사가 미국종합암네트워크 가이드라인으로 권고되어 매우 기쁘게 생각한다”며 “조직검사가 어렵거나 불가능했던 재발 혹은 전이된 전 세계의 유방암 환자들이 더욱 안전하고 정확하게 여성호르몬 수용체 여부를 진단받고 가장 적절한 치료를 받을 수 있을 것으로 기대된다”고 말했다. 이어 “앞으로도 암환자들의 생존율을 높이고 맞춤 치료를 제공하기 위한 글로벌 연구를 주도해 나가겠다”고 덧붙였다. -
 KTC, 의료기기 분야 유럽 수출 확대 지원한다한국기계전기전자시험연구원(KTC)이 의료기기 분야 유럽 수출 확대 지원을 위해 케어젠과 기술 용역 계약을 체결했다고 24일 밝혔다. 이번 계약을 통해 KTC는 케어젠의 유럽 MDR 인증 획득에 필요한 조직수복용 생체재료의 생물학적 안전성을 평가한다. 조직수복용 생체재료란 인체조직 등 대체, 수복, 재건에 사용되는 생체 유래 재료다. KTC는 세포 독성, 감작성, 피내반응, 유전독성, 발열성, 아만성 독성, 이식 시험 등 총 7건의 GLP(비임상시험관리기준) 시험과 생물학적 안전성 평가보고서(BER) 작성을 수행한다. MDR은 유럽 의료기기 수출 시 요구되는 인증으로 2024년 5월 시행을 앞두고 있다. 유럽 의료기기 시장은 2021년 기준 1500억 유로(한화 약 210조원) 규모로 북미 대륙에 이어 세계에서 두 번째로 크다. 또한 1인당 의료기기 시장 규모가 평균 196.7달러로 세계 1위이며 의료기기 수입의존도가 매우 높은 편이다. 이에 국내 기업은 MDR 획득을 통해 유럽 진출을 확대하고자 하지만 기존 의료기기 관리 지침인 MDD보다 취득 비용이 높고 기간이 오래 소요돼 수출에 어려움을 겪고 있다. KTC는 유럽 MDR 인증기관과 업무 협력 관계를 구축해 국내 기업의 유럽 의료기기인증 획득과 차질 없는 해외 시장 진출을 지원할 예정이라고 밝혔다. 한편 KTC는 식품의약품안전처 최다 품목군 지정 시험·검사기관이자 의료기기 제조·품질관리 기준(GMP) 심사기관으로 인허가 토탈 서비스를 제공하고 있다. 또한 국내 최초로 첨단 융복합 의료기기 전용 GLP 시험센터를 세워 국민 안전 확보에 기여하고 있다.
KTC, 의료기기 분야 유럽 수출 확대 지원한다한국기계전기전자시험연구원(KTC)이 의료기기 분야 유럽 수출 확대 지원을 위해 케어젠과 기술 용역 계약을 체결했다고 24일 밝혔다. 이번 계약을 통해 KTC는 케어젠의 유럽 MDR 인증 획득에 필요한 조직수복용 생체재료의 생물학적 안전성을 평가한다. 조직수복용 생체재료란 인체조직 등 대체, 수복, 재건에 사용되는 생체 유래 재료다. KTC는 세포 독성, 감작성, 피내반응, 유전독성, 발열성, 아만성 독성, 이식 시험 등 총 7건의 GLP(비임상시험관리기준) 시험과 생물학적 안전성 평가보고서(BER) 작성을 수행한다. MDR은 유럽 의료기기 수출 시 요구되는 인증으로 2024년 5월 시행을 앞두고 있다. 유럽 의료기기 시장은 2021년 기준 1500억 유로(한화 약 210조원) 규모로 북미 대륙에 이어 세계에서 두 번째로 크다. 또한 1인당 의료기기 시장 규모가 평균 196.7달러로 세계 1위이며 의료기기 수입의존도가 매우 높은 편이다. 이에 국내 기업은 MDR 획득을 통해 유럽 진출을 확대하고자 하지만 기존 의료기기 관리 지침인 MDD보다 취득 비용이 높고 기간이 오래 소요돼 수출에 어려움을 겪고 있다. KTC는 유럽 MDR 인증기관과 업무 협력 관계를 구축해 국내 기업의 유럽 의료기기인증 획득과 차질 없는 해외 시장 진출을 지원할 예정이라고 밝혔다. 한편 KTC는 식품의약품안전처 최다 품목군 지정 시험·검사기관이자 의료기기 제조·품질관리 기준(GMP) 심사기관으로 인허가 토탈 서비스를 제공하고 있다. 또한 국내 최초로 첨단 융복합 의료기기 전용 GLP 시험센터를 세워 국민 안전 확보에 기여하고 있다. -
 바이오 경제 2.0 추진 방향, 환경과 국가경쟁력을 위한 노력저성장, 기후변화, 국가 경쟁력 향상 등의 문제를 해결하기 위한 방안으로 ‘바이오 경제’가 전세계적으로 부상하고 있다. 여기서 바이오 경제란, 바이오 자원에 기반한 공정‧제품‧서비스를 활용하여 경제‧사회의 발전과 지속 가능한 성장을 실현하는 경제 구조를 의미한다. 특히 바이오 경제가 불러올 산업 구조의 변화 및 혁신 기술의 발전 등이 부각되면서 그 중요성은 더욱 커지고 있다. 이에 우리나라 또한 바이오 경제 발전 및 바이오 신산업 육성에 박차를 가하고 있다. 산업통상자원부(이하 산업부)는 기존 의약품 중심의 「바이오 경제 1.0」을 넘어 바이오 신소재, 디지털 바이오 등의 육성을 위하여 「바이오 경제 2.0 추진 방향」을 발표했다. 「바이오 경제 2.0 추진 방향」은 총 5개의 구체적인 발전 방향을 가지고 있다. ▲2030년 세계 1위 바이오의약품 제조국 도약 ▲바이오 신소재 산업 활성화 ▲바이오에너지 상용화 ▲디지털 바이오 혁신생태계 구축 ▲바이오 경제 기반 구축 등 4+1 추진이 그 내용이다. 참고로, 디지털 바이오란 생물학과 정보기술의 융합으로 이루어진 새로운 분야로, 생명체의 유전정보와 생물학적 데이터를 수집, 분석, 응용하는 기술이다. 디지털 바이오 기술을 통하여 질병 치료, 식품 산업 개선 및 바이오 의약품 등 생명과학의 응용이 새롭게 펼쳐질 수 있다. 새로운 방향성을 기반으로 하는 적극적인 바이오 육성 전략을 통해 바이오 경제 경쟁력은 물론, 바이오 수출 또한 크게 향상될 것으로 기대된다. 주요 제약 기업의 바이오의약품부터 바이오의료기기, 바이오 농산물∙화장품 수출 등이 글로벌 시장에서 적극적으로 펼쳐지길 바란다. 위 전략을 추진하기 위해 산업부, 5개 관련 협회, 2개 관계 학회, 4개 산업지원기관 등이 참여하는 ‘바이오 경제 얼라이언스’ 또한 구성되었다. 이를 중심으로 바이오 경제로의 전환과 국가적인 발전이 이루어질 예정이다.
바이오 경제 2.0 추진 방향, 환경과 국가경쟁력을 위한 노력저성장, 기후변화, 국가 경쟁력 향상 등의 문제를 해결하기 위한 방안으로 ‘바이오 경제’가 전세계적으로 부상하고 있다. 여기서 바이오 경제란, 바이오 자원에 기반한 공정‧제품‧서비스를 활용하여 경제‧사회의 발전과 지속 가능한 성장을 실현하는 경제 구조를 의미한다. 특히 바이오 경제가 불러올 산업 구조의 변화 및 혁신 기술의 발전 등이 부각되면서 그 중요성은 더욱 커지고 있다. 이에 우리나라 또한 바이오 경제 발전 및 바이오 신산업 육성에 박차를 가하고 있다. 산업통상자원부(이하 산업부)는 기존 의약품 중심의 「바이오 경제 1.0」을 넘어 바이오 신소재, 디지털 바이오 등의 육성을 위하여 「바이오 경제 2.0 추진 방향」을 발표했다. 「바이오 경제 2.0 추진 방향」은 총 5개의 구체적인 발전 방향을 가지고 있다. ▲2030년 세계 1위 바이오의약품 제조국 도약 ▲바이오 신소재 산업 활성화 ▲바이오에너지 상용화 ▲디지털 바이오 혁신생태계 구축 ▲바이오 경제 기반 구축 등 4+1 추진이 그 내용이다. 참고로, 디지털 바이오란 생물학과 정보기술의 융합으로 이루어진 새로운 분야로, 생명체의 유전정보와 생물학적 데이터를 수집, 분석, 응용하는 기술이다. 디지털 바이오 기술을 통하여 질병 치료, 식품 산업 개선 및 바이오 의약품 등 생명과학의 응용이 새롭게 펼쳐질 수 있다. 새로운 방향성을 기반으로 하는 적극적인 바이오 육성 전략을 통해 바이오 경제 경쟁력은 물론, 바이오 수출 또한 크게 향상될 것으로 기대된다. 주요 제약 기업의 바이오의약품부터 바이오의료기기, 바이오 농산물∙화장품 수출 등이 글로벌 시장에서 적극적으로 펼쳐지길 바란다. 위 전략을 추진하기 위해 산업부, 5개 관련 협회, 2개 관계 학회, 4개 산업지원기관 등이 참여하는 ‘바이오 경제 얼라이언스’ 또한 구성되었다. 이를 중심으로 바이오 경제로의 전환과 국가적인 발전이 이루어질 예정이다. -
 KTR, 강화된 의료기기∙의약품 유럽인증 대비할 새 업무협약 체결KTR(한국화학융합시험연구원)이 폴란드 Pure Clinical과 손을 잡으며 유럽 수출을 위한 임상시험 부담을 완화한다. KTR(한국화학융합시험연구원) 김현철 원장이 13일(현지시간) 진행된 한국-폴란드 비즈니스 포럼에서 폴란드 임상시험기관 퓨어 클리니컬(Pure Clinical) 아담 소반카(Adam Sobantka) 대표와 의료기기 및 의약품 임상시험 협력을 위한 업무협약을 체결했다. 이번 업무협약은 더욱 강화된 MDR의 문제점을 확실히 경감시켜줄 것으로 보인다. MDR은 유럽 의료기기 제도로, 제조사에서 실시하는 전 임상시험부터 인증기관을 거쳐 출판이 이루어질 때까지 제품 전 주기에 걸쳐 적용되는 제도다. 기존 사전 인증보다 더욱 세분화되고 구체화되어 인증 획득이 어려워질 것이라는 우려가 많았다. 강화된 MDR에 따르면 일정 등급 이상의 의료기기와 의약품은 반드시 임상시험을 거쳐야 한다. 또한 인종 간 유전학적 차이에 대한 검증 규정에 따라 임상시험은 유럽 현지인을 대상으로 해야 한다. 한국 진행 임상시험은 인정받지 못하는 만큼, 인허가 소요 비용과 시간 부담이 그만큼 늘어나게 된 것이다. 하지만, 이번 업무협약을 통하여 KTR은 강화된 유럽 의료기기 규정 대응과 의약품 수출 확대를 돕기 위해 유럽 임상시험기관*과 협약을 준비해 왔다. * Pure Clinical: 폴란드 임상시험 종합서비스를 제공하는 임상시험수탁기관(CRO)으로 의료기기 및 의약품에 대한 임상시험과 성능평가 수행. 협약에따라의료기기및의약품유럽수출기업은 KTR을통해폴란드현지에서임상시험을진행하고, 그결과를유럽의료기기규제제도(MDR) 신청에활용할수있게됐다. 특히임상시험을중복진행하지않아도돼인증획득소요시간및비용을크게줄일수있다. 특히 이번 협약으로 KTR은 Pure Clinical과 의약품까지 협력 범위를 넓혀 의약품 수출 기업도 임상시험 부담을 덜 수 있도록 했다. 국내에서주요생산및수출하는제네릭의약품*에대한생물학적동등성시험** 관련협력을약속했다. * 제네릭 의약품: 처음 개발된 ‘원개발 의약품’과 주성분 함량, 복용방법, 효능·효과 품질 등이 동일하게 만들어진 의약품 ** 생물학적 동등성 시험: 제네릭 의약품과 원개발 의약품이 실제 사람의 체내에 흡수되는 속도와 흡수량이 동등하다는 것을 증명하는 시험 이번협약으로의료기기및의약품기업들은유럽임상시험부담을크게줄일수있게될것으로기대된다.
KTR, 강화된 의료기기∙의약품 유럽인증 대비할 새 업무협약 체결KTR(한국화학융합시험연구원)이 폴란드 Pure Clinical과 손을 잡으며 유럽 수출을 위한 임상시험 부담을 완화한다. KTR(한국화학융합시험연구원) 김현철 원장이 13일(현지시간) 진행된 한국-폴란드 비즈니스 포럼에서 폴란드 임상시험기관 퓨어 클리니컬(Pure Clinical) 아담 소반카(Adam Sobantka) 대표와 의료기기 및 의약품 임상시험 협력을 위한 업무협약을 체결했다. 이번 업무협약은 더욱 강화된 MDR의 문제점을 확실히 경감시켜줄 것으로 보인다. MDR은 유럽 의료기기 제도로, 제조사에서 실시하는 전 임상시험부터 인증기관을 거쳐 출판이 이루어질 때까지 제품 전 주기에 걸쳐 적용되는 제도다. 기존 사전 인증보다 더욱 세분화되고 구체화되어 인증 획득이 어려워질 것이라는 우려가 많았다. 강화된 MDR에 따르면 일정 등급 이상의 의료기기와 의약품은 반드시 임상시험을 거쳐야 한다. 또한 인종 간 유전학적 차이에 대한 검증 규정에 따라 임상시험은 유럽 현지인을 대상으로 해야 한다. 한국 진행 임상시험은 인정받지 못하는 만큼, 인허가 소요 비용과 시간 부담이 그만큼 늘어나게 된 것이다. 하지만, 이번 업무협약을 통하여 KTR은 강화된 유럽 의료기기 규정 대응과 의약품 수출 확대를 돕기 위해 유럽 임상시험기관*과 협약을 준비해 왔다. * Pure Clinical: 폴란드 임상시험 종합서비스를 제공하는 임상시험수탁기관(CRO)으로 의료기기 및 의약품에 대한 임상시험과 성능평가 수행. 협약에따라의료기기및의약품유럽수출기업은 KTR을통해폴란드현지에서임상시험을진행하고, 그결과를유럽의료기기규제제도(MDR) 신청에활용할수있게됐다. 특히임상시험을중복진행하지않아도돼인증획득소요시간및비용을크게줄일수있다. 특히 이번 협약으로 KTR은 Pure Clinical과 의약품까지 협력 범위를 넓혀 의약품 수출 기업도 임상시험 부담을 덜 수 있도록 했다. 국내에서주요생산및수출하는제네릭의약품*에대한생물학적동등성시험** 관련협력을약속했다. * 제네릭 의약품: 처음 개발된 ‘원개발 의약품’과 주성분 함량, 복용방법, 효능·효과 품질 등이 동일하게 만들어진 의약품 ** 생물학적 동등성 시험: 제네릭 의약품과 원개발 의약품이 실제 사람의 체내에 흡수되는 속도와 흡수량이 동등하다는 것을 증명하는 시험 이번협약으로의료기기및의약품기업들은유럽임상시험부담을크게줄일수있게될것으로기대된다.


![[특집-ISO/IEC JTC 1/SC 17 활동] 35. Result of voting on SR Ballot for ISO/](http://www.stdnews.kr/data/file/news/thumb/thumb-3555379571_4cufp2BH_756bcefa64e6169e58646ad7b061ecbec455fb11_340x240.jpg)
![[특집-ISO/IEC JTC 1/SC 17 활동] 34. Result of voting on SR ballot for ISO/](http://www.stdnews.kr/data/file/news/thumb/thumb-3555380113_kIQxAlfN_727cc6e35ccb9d5e6c07574a3b3a2ab9db104d48_340x240.jpg)
![[특집-ISO/IEC JTC 1/SC 17 활동] 33. Result of voting on SR ballot for ISO/](http://www.stdnews.kr/data/file/news/thumb/thumb-32068165_R52GPIij_2bca2660198a937d2534db7bfd9fc8174a76cfa2_340x240.jpg)
![[특집-ISO/IEC JTC 1/SC 17 활동] 32. Result of voting on SR Ballot for ISO/](http://www.stdnews.kr/data/file/news/thumb/thumb-32068165_TxRrtYEa_c36d1a53acc15db7e18fae132ffef64e11bda43c_340x240.jpg)
![[특집-ISO/IEC JTC 1/SC 17 활동] 31. Result of voting on SR Ballot for ISO/](http://www.stdnews.kr/data/file/news/thumb/thumb-3555377690_nrjmWhSf_d9b63299e7f3f52053141cae28f32f7df40b5918_340x240.jpg)


![[일본] 요코하마(横浜), 3월 원격근무로 일하는 50대 여성이 장시간 노동을 강요받아 적응장애가 발병해 산재로 인정받아](http://www.stdnews.kr/data/file/news/thumb/thumb-3555377672_BapV2SmF_41a011a26290be1daa3f6a5220df7b8b6d167f69_340x240.jpg)
![[인도] 마하라슈트라주 식품의약국(Maharashtra FDA), 맥도날드 상품명에 치즈를 잘못 표기해 소비자 기만 지적](http://www.stdnews.kr/data/file/news/thumb/thumb-3743818281_Uu5GpcKZ_6890f33f4b087f58686ed20e46a04bbb79ad883e_340x240.jpg)
![[남아공] 토코만 푸드(Thokoman Foods), 자사 땅콩버터 식품 안전성 재확인](http://www.stdnews.kr/data/file/news/thumb/thumb-3743818281_h5HrK0kT_c2453abdb4577a16b34590f5b8f76de9c2a95469_340x240.jpg)
![[일본] 혼다(ホンダ), 2030년까지 전기자동차(EV)를 중심으로 하는 전동화와 소트프웨어 개발에 10조 엔을 투자할 계획](http://www.stdnews.kr/data/file/news/thumb/thumb-3555381172_1g5z7YDN_4db7699b271b5e9dbbe1a4f6dc69fb01a9881abb_340x240.jpg)
![[일본] 자민당(自民党), 기업이 직원을 고객의 '카스하라(カスハラ)로부터 보호를 의무로 하는 방안을 고려 중](http://www.stdnews.kr/data/file/news/thumb/thumb-3555381172_PCNyaL1v_9f9b79d526b4be07024401e874fe26f618a42e7c_340x240.jpg)
![[일본] 총무성(総務省), 2023년 기준 전국의 빈집은 900만 호로 사상 최고치 기록](http://www.stdnews.kr/data/file/news/thumb/thumb-3555379571_qr01mWC9_fef7fa874e596585a04ee2dae235376595341779_340x240.jpg)
![[특집-기상기후재난] 한국중부발전(주) 신정철 선임 인터뷰 - 행정안전부 뿐 아니라 기상기후 연계조직 모두가 참여하는 협의체가](http://www.stdnews.kr/data/file/news/thumb/thumb-3555374516_iKWwUBas_9c1729f1e3977ee50c398986e7f98d5002a57deb_340x240.jpg)
![[특집-기상기후재난] (주)비밍코어 정성민 대표 인터뷰 - 인공지능(AI) 활용한 기후재난 대처 솔루션 개발](http://www.stdnews.kr/data/file/news/thumb/thumb-3555374391_0JZYhIcj_dca23c54fc7923952082a9d7af92db00b9dd33c9_340x240.jpg)
![[기획-표준 전문가] 한국투자증권 김범수 FC 인터뷰 - 표준전문가 양성 교육이 지속되길 희망](http://www.stdnews.kr/data/file/news/thumb/thumb-3555374114_Np9hM7aC_e6ffa916aade15e1c301badf3132ed3f0551a900_340x240.jpg)
![[특집-기상기후재난] 행정안전부 안전교육 전문인력 유정희 강사 인터뷰 - 기상기후재난예방 전문가 양성 시급](http://www.stdnews.kr/data/file/news/thumb/thumb-3555374240_gOmdLG10_cfc17ed887dccc93f503013bf794ed568a5d40dc_340x240.jpg)
![[특집-기상기후재난] (주)이토스 김형식 대표 인터뷰 - 재난을 사전에 예측·예방할 기술개발 시급](http://www.stdnews.kr/data/file/news/thumb/thumb-32068165_lmUrCBIn_797dc8926bb7d90542546463cc73e6233f0bbb46_340x240.png)